ГЛАВА 17. ОСНОВНЫЕ ПРИНЦИПЫ МОЛЕКУЛЯРНО-КИНЕТИЧЕСКОЙ ТЕОРИИ
Рассмотренная смесь газов близка по составу к обычному атмосферному воздуху.
Любой из нас прекрасно чувствует, что значит горячо или холодно, но дать точное определение температуры не так-то просто. Недаром физики окончательно поняли, что это за величина, только к середине 19 века через 150 лет после Ньютона. Чтобы понять это определение, давайте перечислим, что мы знаем о температуре и каковы основные свойства этой величины. Главное ее свойство заключается в том, что при контакте тел с разными температурами происходит выравнивание их температур, причем, вообще говоря, без перемещений макроскопических количеств вещества. А поскольку при контакте тел их молекулы сталкиваются друг с другом, то для определения температуры необходимо найти такую механическую характеристику, которая выравнивается в процессе хаотических столкновений молекул.
В середине XIX в. Л. Больцман, рассматривая статистику столкновений молекул доказал, что если два газа привести в тепловой контакт, то через некоторое время установится такое состояние, когда средние кинетические энергии поступательного движения молекул газов станут одинаковыми. А это означает, что температура T связана со средней кинетической энергией поступательного движения молекул. Больцман предположил, что эта связь должна быть максимально простой, т.е. представлять собой прямую пропорциональную зависимость
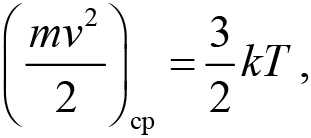
где k — коэффициент пропорциональности, который называется постоянной Больцмана. Значение постоянной Больцмана зависит от выбора единиц измерения температуры. Если в качестве таковых используются градусы Кельвина (или просто Кельвины — К), постоянная Больцмана равна


