ГЛАВА 20. ВНУТРЕННЯЯ ЭНЕРГИЯ ГАЗА. ПРЕВРАЩЕНИЯ ЭНЕРГИИ В ТЕПЛОВЫХ ПРОЦЕССАХ. ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
В результате первый закон термодинамики позволяет установить связь между количеством сообщенной газу теплоты и изменениями его макроскопических параметров. Рассмотрим еще один пример.
Пример 20.3. Некоторое количество идеального одноатомного газа участвует в процессе, в ходе которого сначала давление газа изохорически увеличивается в n = 2 раза, а затем его объем изобарически увеличивается в k = 3 раза. Какое количество теплоты сообщают газу в указанном процессе? Начальное давление и объем
газа ![]() =105 Па и
=105 Па и ![]() =100 л соответственно.
=100 л соответственно.
Решение. Будем использовать первый закон термодинамики (20.7)
![]()
для рассматриваемого процесса. Изменение внутренней энергии газа найдем по формуле (20.2) и закону Клапейрона-Менделеева
где ![]() - количество вещества рассматриваемого газа;
- количество вещества рассматриваемого газа; ![]() и
и ![]() - начальная и конечная температуры газа.
- начальная и конечная температуры газа.
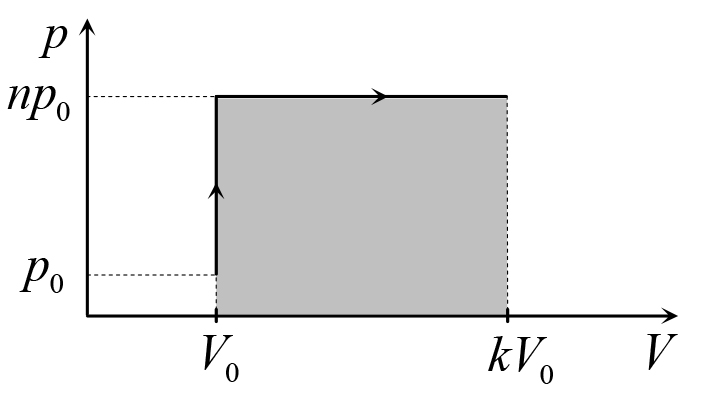
Рис. 20.4
Для того чтобы найти работу газа построим график исследуемого процесса в координатах p – V. Этот график приведен на рис. 20.4. Работа газа представляет собой площадь под графиком процесса, то есть площадь фигуры, выделенной на рис. 20.4. Из графика находим
Подставляя приращение внутренней энергии газа (20.17) и работу газа (20.18) в первый закон термодинамики, найдем количество теплоты, сообщенное газу в исследуемом процессе
![]()


