ГЛАВА 20. ВНУТРЕННЯЯ ЭНЕРГИЯ ГАЗА. ПРЕВРАЩЕНИЯ ЭНЕРГИИ В ТЕПЛОВЫХ ПРОЦЕССАХ. ПЕРВЫЙ ЗАКОН ТЕРМОДИНАМИКИ
Давления ![]() - равны расстояниям от оси объемов до графика в тех его точках, где приращение объема газа равнялось
- равны расстояниям от оси объемов до графика в тех его точках, где приращение объема газа равнялось ![]() . Поэтому произведения
. Поэтому произведения ![]() имеют смысл площади малого прямоугольника с основанием
имеют смысл площади малого прямоугольника с основанием ![]() и высотой
и высотой ![]() (один из таких прямоугольников выделен на рис. 20.2). Поэтому работа газа представляет собой площадь фигуры, лежащей под графиком зависимости давления от объема в рассматриваемом процессе (со знаком «+» при расширении газа, со знаком «-» при сжатии). Отсюда следует, что если процесс, происходящий с газом, определен, то есть известна зависимость давления газа от его объема в этом процессе, то работа газа может быть вычислена, как площадь фигуры под графиком зависимости p(V). В частности, можно определить работу газа, совершенную в любом изопроцессе. Например, работа газа в изобарическом процессе равна
(один из таких прямоугольников выделен на рис. 20.2). Поэтому работа газа представляет собой площадь фигуры, лежащей под графиком зависимости давления от объема в рассматриваемом процессе (со знаком «+» при расширении газа, со знаком «-» при сжатии). Отсюда следует, что если процесс, происходящий с газом, определен, то есть известна зависимость давления газа от его объема в этом процессе, то работа газа может быть вычислена, как площадь фигуры под графиком зависимости p(V). В частности, можно определить работу газа, совершенную в любом изопроцессе. Например, работа газа в изобарическом процессе равна
где p - давление газа (постоянное в течение изобарического процесса); ![]() - приращение его объема в этом процессе (не обязательно малое).
- приращение его объема в этом процессе (не обязательно малое).
После того как приращение внутренней энергии газа и его работа вычислены по первому закону термодинамики можно определить количество тепла, сообщенное газу. Рассмотрим один пример.
Пример 20.2. Одноатомный идеальный газ расширяется из некоторого начального состояния с объемом ![]() до объема
до объема ![]() один раз изотермически, второй изобарически, третий адиабатически. В каком процессе газ совершает бoльшую работу? Получает большее количество теплоты?
один раз изотермически, второй изобарически, третий адиабатически. В каком процессе газ совершает бoльшую работу? Получает большее количество теплоты?
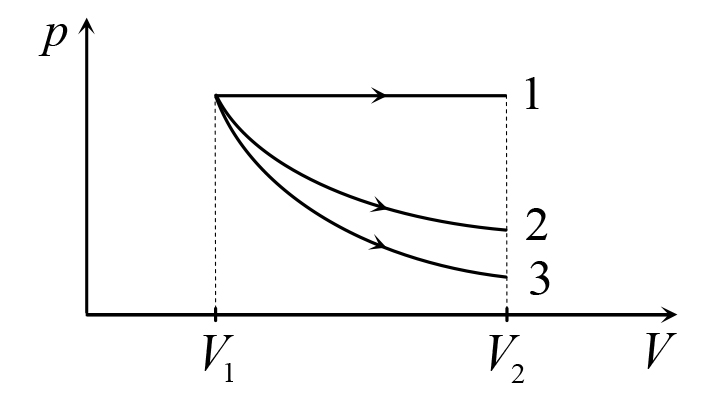
Рис. 20.3
Решение. Чтобы сравнить работы, совершенные газом, построим графики зависимости давления от объема в указанных процессах и сравним площади под этими графиками. При изобарическом расширении давление не изменяется, поэтому график зависимости p(V) - горизонтальная прямая (зависимость 1 на рис. 20.3).


