ГЛАВА 36. АТОМНАЯ И ЯДЕРНАЯ ФИЗИКА
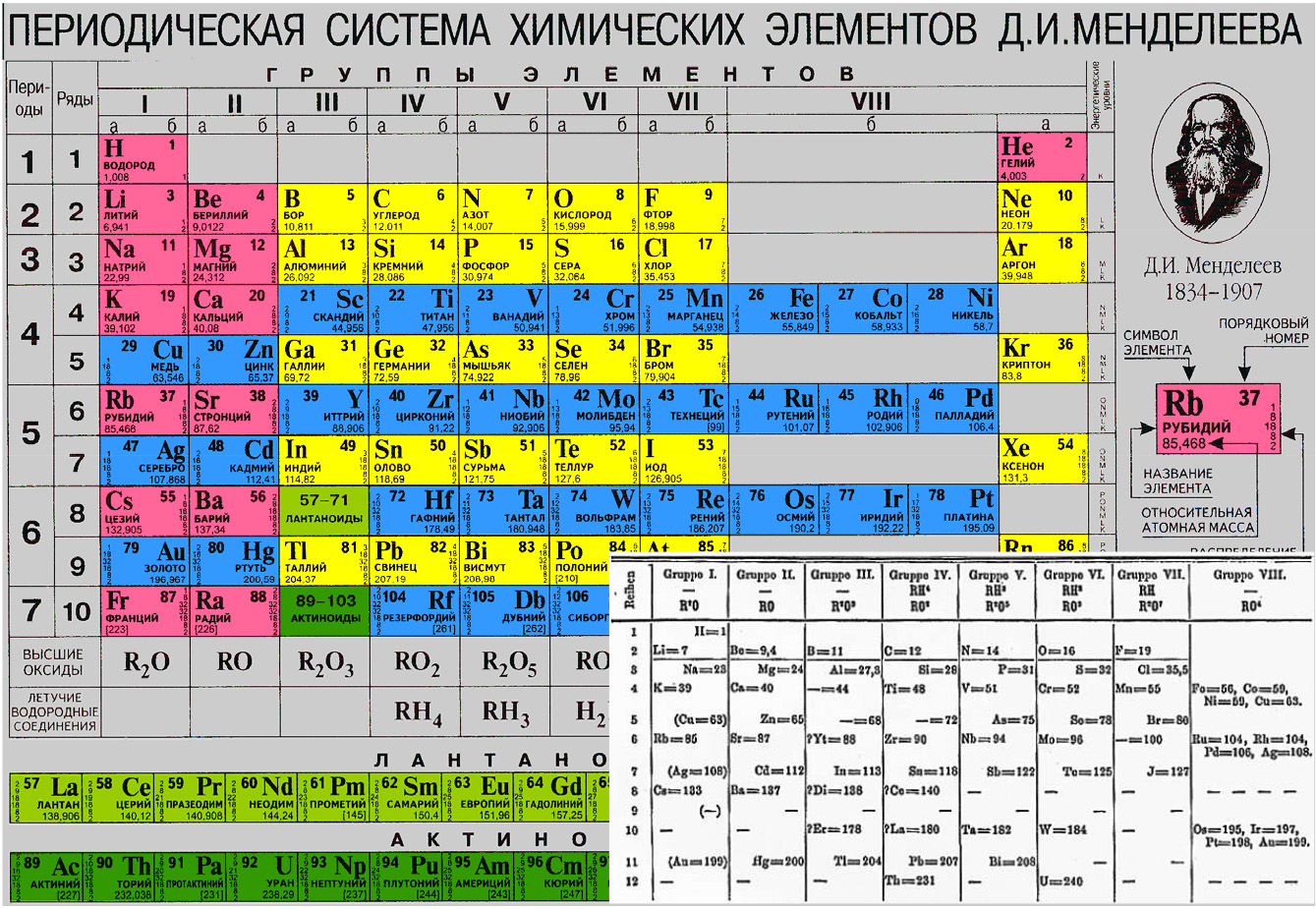
Периодическая таблица (система) химических элементов, предложенная Д.И. Менделеевым в 1869 г. (внизу справа — вариант таблицы самого Менделеева 1871 г.). Периодичность свойств элементов является отражением повторяемости конфигурации валентных электронов (которые и определяют химические свойства) при увеличении их количества, т.е. при переходе от одного элемента к другому.
Важнейшими открытиями, которые позволили построить первые модели атомов, были открытия электрона и радиоактивности. При исследовании прохождения электрического тока через сильно разреженные газы были открыты частицы, испускаемые катодом разрядной трубки, обладающие свойством отклоняться в электрическом и магнитном полях. Выяснилось, что эти частицы, которые были названы электронами, заряжены отрицательным зарядом. В 1897 английский физик Дж.Дж. Томсон1 измерил отношение заряда этих частиц к их массе.
1 У фамилии первооткрывателя электронов Дж.Дж. Томсона всегда пишут оба инициала, чтобы не путать его с другим известным физиком — Дж.П. Томсоном — сыном Дж.Дж. Томсона. Оба они были удостоены Нобелевской премии — Дж.Дж. Томсон за теоретические и экспериментальные исследования прохождения электричества через газы, приведшие к открытию электрона (1906 г.), Дж.П. Томсон — за открытие дифракции электронов на кристаллах (1937 г.).


